【今日药闻】
国家药监局:修订静注人免疫球蛋白说明书
1 月 15 日,国家药品监督管理局发布 2019 年第 1 号公告,决定对静注人免疫球蛋白(pH4)和冻干静注人免疫球蛋白(pH4)说明书增加警示语,并对【不良反应】、【注意事项】、【老年用药】等项进行修订。
据了解,静注人免疫球蛋白的适应症包括原发性免疫球蛋白缺乏症、新生儿败血症、重型原发性免疫性血小板减少症、川崎病、全身型重症肌无力、急性格林巴利综合征。目前被多个地方列入重点监控目录。
静注人免疫球蛋白 (pH4) 与冻干静注人免疫球蛋白 (pH4) 均属于国家医保乙类产品。米内网数据显示,静注人免疫球蛋白 (pH4) 国产批文数共计 85 个,生产企业 26 家;冻干静注人免疫球蛋白 (pH4) 国产批文 22 个,共计 11 个厂家生产
国家药监局:修订养血清脑颗粒(丸)非处方药说明书范本
具体内容,查看原文。
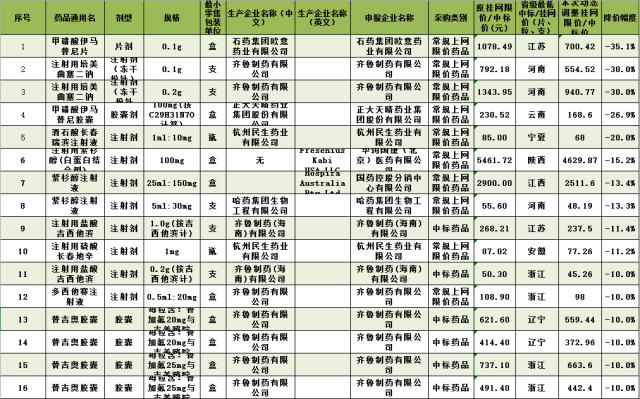
103 个抗癌药大降价,最大降幅 35%
1 月 15 日,四川药械采购监管网发布了关于执行第三批挂网抗癌药动态调整结果的通知,对申请限价动态调整的 103 个药品的中标/挂网价予以价格调整,其中涉及石药、正大天晴、齐鲁制药、恒瑞、辉瑞等 25 家知名药企。

附:降幅超过 10% 的名单
【新药信息】
FDA 新药回顾:诺华成为过去 10 年最大赢家,共 17 个新药获
福布斯网站健康频道专栏作家 Bernard Munos 近日发表文章,对美国 FDA 批准的新药进行了回顾。文章指出,2018 年对于制药行业而言注定是不平凡的一年。在这一年,美国食品和药物管理局(FDA)共批准了 61 个新药,其中 FDA 药物评估和研究中心(CDER)批准了 59 个,另外两个是由 FDA 生物制品评估和研究中心(CBER)批准的重组疗法(Andexxa 和 Jivi)。
【数据更新& 指南推荐】
今日更新说明书 53 条,新增 11 条,指南 16 部。在更新的指南中,我们挑选了以下 4 部指南推荐阅读:
《2019KSHF 指南:急性心衰的管理:第 3 部分—急性心衰的具体管理》
《2018 专家共识:高尿酸血症和高心血管风险患者的诊断和治疗》
【用药热议】
最近在丁香园论坛里有位站友求助:说明书里的不宜配伍具体是什么意思?
配伍禁忌、不能配伍、单独使用,这些又都是什么意思?严格来说这些不是同一个意思吗?你怎么看?
【推荐阅读】
------------------------------------------------
也欢迎各位药粉为我们提供更多建议,联系方式:
用药助手官方微博:用药助手
用药助手官方公众号:DrugsApp
用药助手官方客服号:dxy_drugs;dxy-drugs1
