三、预防和治疗 CKD 中的骨折
1.CKD 患者现有的治疗方法
对 CKD1~3b 期的患者而言,预防骨折的方法和没有 CKD 的骨质疏松的患者一样。每个病例都推荐纠正低 25OHD。eGFR>30 ml /min/1.73m2的患者,和非 CKD 患者一样推荐雷洛昔芬、双磷酸盐类药物和特立帕肽(人重组 PTH)。但应谨慎使用雷洛昔芬,因其在 CKD 中与血栓形成风险增加有关。
对 CKD4~5D 期的骨质疏松患者的治疗是个挑战。2017 年的 KDIGO 指南推荐,对 CKD-MBD 生化指标异常以及低 BMD/脆性骨质的 CKD3a~5D 期患者,治疗选择应该考虑生化异常的强度和可逆性、CKD 的进展以及骨活检的结果。因此,在纠正了骨矿化的生物标志物之后,在开始抗骨折治疗之前,应该继续随访 6~12 个月。
我们的意见是,仅仅只是低 BMD 的患者不应该治疗,因为没有证据表明抗骨折治疗的有效性。应首先治疗骨质疏松性骨折的患者,因为他们骨质脆弱。第一步应该明确骨折的病因。这可能是由于骨矿化缺陷造成的,虽然骨矿化缺陷在普通人群中很少见,但是在 CKD 患者中却很常见。
较低的血清 25OHD 和血钙水平、同步较高的碱性磷酸酶水平提示骨软化症,需要骨活检证实。没有低钙血症时,骨软化症也可能与低磷血症(严重的限磷饮食、过度透析、甲状旁腺切除术或酗酒)有关。口服维生素 D 或磷或透析液中加磷可以逆转临床和生化指标。如果没有低血钙或低血磷,那么可能是其它病因引起的骨软化症,如在骨活检标本中测定到较高的氟含量。
大多数抗骨折治疗方案在 eGFR<30 ml/min/1.73m2的患者中都禁忌使用。不管肾功能如何,双磷酸盐类药物会蓄积在骨组织中,肾脏清除率降低的情况下蓄积就增多。这与骨矿化缺陷和骨软化症有关,或者会导致 ABD。由于这个原因,没有合适的随机对照试验评估过这些药物在 CKD 骨折中的作用。
少量的研究和早期的事后分析显示,使用双磷酸盐类药物会引起 BMD 增加,但不足以降低骨折的风险。近期的一项系统回顾发现没有证据表明这些药物治疗在 CKD 中有帮助。小剂量的双磷酸盐类药物可能是另一种治疗选择,但仍有待临床试验来证实。
最近,狄诺塞麦(一种 NF-κB 配体的抗核受体激活剂)为治疗骨质疏松和骨脆性增加燃起了希望。狄诺塞麦在骨质疏松的妇女中降低了椎体骨折、非椎体骨折和髋关节骨折的风险。在 CKD4 期的女性患者中,狄诺塞麦增加了 BMD,增加程度与 CKD1~3 期类似,但至今尚不能下降低骨折风险的结论。
在 CKD4~5D 期的严重甲旁亢患者中,狄诺塞麦可能促进了显著的低钙血症,并且在 15 天内升高 PTH 水平,因此在 CKD 患者中给予充狄诺塞麦时需要补充钙剂,并严密监测这些潜在的不良反应。目前正在骨质疏松的 CKD5D 期女性患者中进行临床试验(NCT 01464931),将会为狄诺塞麦对 BMD 和矿物质代谢的影响提供答案。更重要的是,未来的试验应该评价狄诺塞麦对骨折风险的影响。
2. 骨折的治疗
对 CKD 患者的骨折治疗,目前没有明确的指南推荐意见。这里提供一些基于我们自己临床经验的指南推荐(图 3)。由于无论循环中骨的生物标志物水平如何都会发生骨折,因此治疗决策首先需要纠正矿物质代谢紊乱。
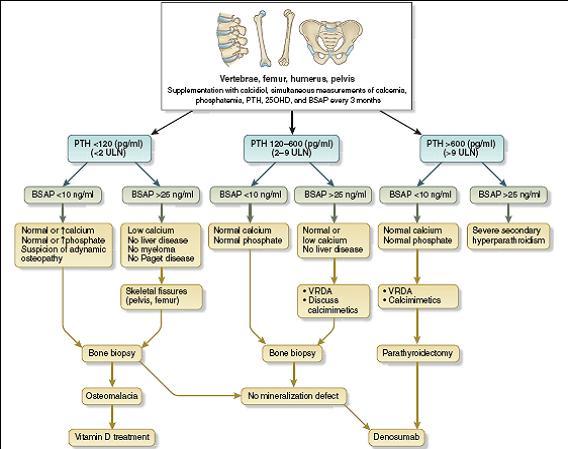
图 3 骨折的治疗指南
在高 PTH 水平的患者中,降低 PTH 水平有助于改善骨的状态。在继发性甲旁亢的老年透析患者中,西那卡塞能有效降低骨折率。因此我们推荐首先降低 PTH 水平以减少骨皮质的流失,降低外周骨折的风险。由于缺乏在高 PTH 情况下使用狄诺塞麦的数据,考虑在 PTH 水平正常的情况下再使用狄诺塞麦。
主要的问题在于在低 PTH 水平的患者中如何治疗骨折。有些担心抗骨吸收治疗会进一步降低本已较低的骨重建率。在非 CKD 患者中,无论骨转运类型如何,狄诺塞麦都有效地降低了骨质疏松患者的骨折率,这表明在低转运性骨病中狄诺塞麦也有抗骨折效应,并且独立于骨的重建率。
在没有肾功能衰竭的绝经后女性中,狄诺塞麦不促进主动脉的钙化。需要进行试验来明确狄诺塞麦这一药物对 CKD 中的血管钙化有无影响。另外,在透析患者中使用狄诺塞麦应该严密监测随访血管钙化。
对骨质疏松最佳的治疗是提高骨的形成以恢复骨量。目前几乎没有合成代谢方面的治疗手段。特立帕肽的作用仅在 7 例血透患者的小规模试验中进行了研究,发现 7 例患者中有 6 例患者在经过 6 个月的特立帕肽治疗后,腰椎和股骨的 BMD 显著增加。对于特立帕肽预防骨折的效果还一无所知,并且禁用于有癌症病史的患者。
抗硬化蛋白抗体是一种有前景的合成药物,它通过与硬化蛋白(Wnt 通路的一种天然拮抗剂)结合促进骨形成。Romosozumab 在没有 CKD 的绝经后女性中增加了 BMD,预防了骨折。有趣的是,抗硬化蛋白抗体仅仅增加了低 PTH 水平的 CKD 大鼠的骨形成和骨量,而非高 PTH 水平的 CKD 大鼠。虽然还要等待更多的实验数据,但是这一新药燃起了新的希望,并且为根据 CKD 中的骨转运率而制定个性化治疗提供了武器。
四、结论
CKD 患者中较高的骨折发生率和死亡率需要新的工具来评估骨折风险。亟需在 CKD 人群中开展纳入骨活检和影像学数据的预防和治疗骨折的 RCT 研究。由于 CKD 中骨脆性的复杂性,在开始抗骨吸收治疗或未来新的合成代谢治疗之前,应该开展肾病专家和骨科专家的多学科讨论。
